ما هي المركبات الأمفوتيرية؟
تم التدقيق بواسطة: فريق أراجيك
المركبات الأمفوتيرية هي جزيئات أو أيونات متذبذبة من الممكن أن تتفاعل كحمض أو كقاعدة، وكلمة أمفوتيرية مشتقة من الكلمة اليونانية Amphoteroi والتي تعني كلا النوعين أو كلاهما.
تُعرف أكاسيد المعادن التي تتفاعل مع الأحماض والقواعد لإنتاج الأملاح والماء بأكاسيد الأمفوتريك، وتشمل أكاسيد الأمفوتريك على أكسيد الرصاص وأكسيد الزنك من بين العديد من الأنواع الأخرى.
ما هي المركبات الأمفوتيرية بالأمثلة؟
ومن الأمثلة على سلوك التفاعلات الأمفوتيرية:
- تفاعل الماء مع الحمض: H2O + HCl ⇌ H3O+ + Cl–
- تفاعل الماء مع القاعدة: H2O + NH3 ⇌ NH4+ + OH–
- تفاعل هيدروكسيد البريليوم مع الحمض: Be(OH)2(s) + H2S04(aq) → BeS04(s) + 2H2O(l)
- تفاعل هيدروكسيد البريليوم مع القاعدة: Be(OH)2(s) + 2OH–(aq) → [Be(OH)4]2-(aq)
- تفاعل أكسيد الألومنيوم مع الحمض: Al2O3(s) + 6H30+(aq) + 3H2O(l) → 2[Al(OH2)6]3+(aq)
- تفاعل أكسيد الألمنيوم مع القاعدة: Al2O3(s) + 2OH–(aq) + 3H2O(l) → 2[Al(OH)4]–(aq)
- تفاعل أكسيد الزنك مع الحمض: ZnO + H2SO4 → ZnSO4 + H2O
- تفاعل أكسيد الزنك مع القاعدة: ZnO + 2 NaOH + H2O → Na2[Zn(OH)4]
يمكن استخدام هذا التفاعل لفصل المركبات المختلفة مثل الزنك الذي يذوب في القاعدة عن المنغنيز الذي لا يذوب في القاعدة.
- تفاعل أكسيد الرصاص مع الحمض: PbO + 2 HCl → PbCl2 + H2O
- تفاعل أكسيد الرصاص مع القاعدة: PbO + 2 NaOH + H2O → Na2[Pb(OH)4]
- تفاعل أكسيد ستانوس مع الحمض: SnO +2 HCl ⇌ SnCl2 + H2O
- تفاعل أكسيد ستانوس مع القاعدة: SnO +4 NaOH + H2O ⇌ Na4[Sn(OH)6]
ومن المواد الامفوتيرية ما يلي:
الماء والأحماض الأمينية وأيونات كربونات الهيدروجين وأيونات كبريتات الهيدروجين وهي مثال مهم على المواد المتذبذبة.
أكاسيد المعادن والفلزات والهيدروكسيدات بما في ذلك: الألومنيوم والزرنيخ و البريليوم والكوبالت والكروم والنحاس والغاليوم والجرمانيوم والذهب والحديد والفضة والتيلوريوم والقصدير والزنك والبزموت والأنتيمون.
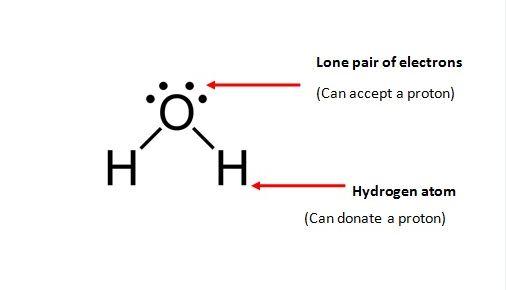
يحتوي جزيء الماء على ذرات هيدروجين وبالتالي يمكن أن يعمل كحمض في التفاعل، وتحتوي ذرة الأكسجين في الماء على زوجين منفصلين وبالتالي يمكن استخدام أحدهما لتكوين رابطة مع (H+)، لذلك من الممكن أن يعمل جزيء الماء كقاعدة في التفاعل فهو لديه القدرة على العمل كحمض أو كقاعدة لذلك هو مذبذب.
ما علاقة الجزيئات البرمائية بالمركبات الأمفوترية؟
الجزيئات البرمائية هي نوع من أنواع الامفوتريك التي إما تتبرع ببروتون أو تقبله حسب الظروف، وليس كل الجزيئات الأمفورماتية هي جزيئات برمائية، فمثلًا: أكسيد المعدن Zno لا يحتوي على الهيدروجين ولا يمكنه التبرع بالبروتون،
وفقًا لنظرية برونستد_ لوي للأحماض والقواعد فإن الأحماض تمنح البروتونات، أما القواعد فهي مستقبلة للبروتونات، ويمكن لجزيء أمفبروتيك ( أو الأيون) إما التبرع أو قبول البروتون أي إنه يعمل إما كحمض أو كقاعدة،
تميل أكاسيد هيدروكسيدات المعادن إلى أن تكون أساسية ضعيفة وتعطي طبيعة متذبذبة، ومعظم هذه المركبات قابلة للذوبان بشكلٍ طفيف في الماء لدرجة أن طابعها الحمضي أو الأساسي واضح فقط في تفاعلها مع الأحماض والقواعد القوية، وبشكلٍ عام تميل هذه المركبات إلى أن تكون أساسية أكثر من أن تكون حمضية، و بالتالي تتحلل أكاسيد وهيدروكسيدات الألومنيوم والحديد والزنك في محلول حمضي خفيف.
Al(OH)_3 +3 H^+\rightarrow Al^{3+}(aq) +3H_2O
(Al(OH)_3 (s) + OH^- \rightarrow Al(OH)_4^- (aq
ما هو شكل المركبات الأمفوتيرية؟
المركبات الأمفوتيرية هي المركبات القادرة على أخذ دور الحمض (تقبل زوج من الالكترونات) عند التفاعل مع المواد الأساسية، وعلى أخذ دور الأساس (تقبل البروتونات) عند التفاعل مع المواد الحمضية، أي باختصار يمكن أن تكون حمض أو أساس وذلك حسب خواص الوسط المحيط الموجودة فيه، يمكن أن تكون هذه المركبات على شكل أيونات أو عناصر أو جزيئات، وأهم مثال على المركبات الأمفوتيرية هو الماء، والأحماض الأمينية وأكاسيد المعادن.
ويمكن أن تشكل المركبات العضوية مركبات أمفوتيرية، وأهم مثال على ذلك هو الأحماض الأمينية والبروتينات، على سبيل المثال، الجلايسين، صيغته الكيمائية NH2.CH2.COOH، والذي يعتبر بحكم وجود المجموعة NH2 أساس لا مائي، ويعتبر بنفس الوقت بحكم وجود مجموعة COOH حمض عضوي عادي، وعند إذابة مثل هذه المادة في الماء، فإنها تتأين كحمض، وكأساس، ويتكون الملح من معادلتها المتبادلة.
الماء كمركب أمفوتيريك
يلعب الماء دور حمض لاحتوائه على ذرات الهيدروجين، ويلعب دور أساس لأن ذرة الأوكسجين بداخله تحتوي على الكترونين حرين في طبقتها السطحية، وبالتالي تستطيع منحهما لتكوين رابطة مع الهيدروجين H+، وتلعب دور الأساس حسب قاعدة برونشتد ولوري.
عند وجود الماء في وسط حمض تكون المعادلة كالتالي:
H2O + HCl → H3O+ + Cl
وعند وجوده في وسط قلوي يلعب الماء دور حمض وتكون المعادلة كالتالي:
H2O + NH3 → NH4+ + OH
وبحسب ما هو متعارف عليه في الكيماء، تعمل كل المركبات التي تحتوي زمرة هيدروكسيد كأساس، ولكن وجد مؤخرًا أن بعضها يمكن أن يلعب دور الحمض والأساس بنفس الوقت، وأشهر مثال على المركبات الأمفوتيرية التي تحتوي زمرة هيدروكسيد هو هيدروكسيد الألومنيوم، ونوضح ذلك في التفاعلات التالية.
تفاعل هيدروكسيد الألمنيوم في محلول حمضي
نعلم أن Al (OH) 3 غير قابل للذوبان بشكل جيد في الماء؛ ومع ذلك، في محلول شديد الحمضية يتغير الوضع، على سبيل المثال، نذكر تفاعل هيدروكسيد الألمنيوم Al (OH) 3 مع حمض كلور الماء HCl:
HCl (aq) + Al (OH) 3 (aq) AlCl3 (aq) + 3H2O (l)
يعتبرالتفاعل السابق مثالًا كلاسيكيًا لتفاعل حمض وأساس مما ينتج عنه ماء نقي وملح كلوريد الألمنيوم AlCl3.
تفاعل هيدروكسيد الألمنيوم في المحلول الأساسي
Al (OH) 3 (aq) + OH (aq) Al (OH)4 (aq)
هنا، يلتقط هيدروكسيد الألومنيوم أيون الهيدروكسيد من المحلول، وبالتالي يعمل كحمض.
إذاً يمكن أن تكون هيدروكسيدات المعادن ذات الذرات المعدنية المركزية والمشحونة بشحنات كبيرة من المركبات الأمفوتيرية، وبالإضافة إلى الألومنيوم، يمكن أن تشكل المعادن مثل: الزنك والقصدير والرصاص والبريليوم أكاسيد أمفوتيرية أو هيدروكسيدات. يعتمد ما إذا كانت هذه الهيدروكسيدات تتصرف كأحماض أو قواعد على الرقم الهيدروجيني لمحلول الوسط المحيط، وعلى خواصه الأخرى، ويستفاد من المركبات الأمفوتيرية بكثرة في الكثير من مجالات الكيمياء التطبيقية.
 LEAP26
LEAP26 ASUS
ASUS RØDE
RØDE REDMAGIC
REDMAGIC TV
TV Partner With Us
Partner With Us