ما هي طرق انتقال الحرارة

تم التدقيق بواسطة: فريق أراجيك
تعتبر الحرارة والقوانين المتعلّقة بها من القواعد الأساسيّة في نظام الحياة في هذا الكون وأحد الركائز الهامّة في معظم العلوم الفيزيائيّة الأخرى. وعلى الرغم من أننا قليلًا ما نلاحظ وجود الحرارة وتبدّلاتها وطرق انتقالها، إلّا أنّها تحيط بنا وموجودة في معظم دقائق وتفاصيل حياتنا اليوميّة. فما هي الحرارة بالضبط؟ وما هي طرق انتقالها؟ وما صلتها بعلم الترموديناميك؟ سنجيب في مقالنا هذا عن هذه التساؤلات ونستعرض أهم التفاصيل المتعلّقة بمفهوم انتقال الحرارة في الأوساط المختلفة.
ما هي الحرارة

كما نعلم فإن الحرارة هي شكلٌ من أشكال الطاقة، وهي تتولّد على مستوى جُزيئات المادّة، فعندما تكتسب المادّة ما طاقةً بمقدارٍ معيّنٍ فإنّ جُزيئاتها تبدأ بالاهتزاز في مكانها، سواءً أكانت هذه الجُزيئات ثابتة (جسم ثابت) أم متحرّكة (جسم متحرّك). هذه الجُزيئات المهتّزة تنقل بدورها الطاقة (الاهتزاز) إلى الجُزيئات المجاورة لها مسبّبةً اهتزازها أيضًا.
وكلما كانت الطاقّة التي تُزوَّد بها
الجُزيئات أكبر كلما كانت الحركة الاهتزازيّة أكثر شدّةً. وعندما تبلغ طاقة هذه
الجُزيئات حدًّا معيّنًا (كدرجة الذوبان أو الغليان مثلًا) فإنّها تتحرّر من
الروابط والقوى الداخليّة المقيّدة لها وتُغيّر بذلك طورها أو حالتها الفيزيائيّة
(كالانتقال من الحالة الصلبة إلى الحالة السائلة أو من الحالة السائلة إلى
الغازيّة).
ويمكن للطاقة الحراريّة أن تنتقل من مادّةٍ لأخرى أو حتى ضمن المادّة ذاتها عند وجود فروقٍ في درجات الحرارة (تُقاس درجات الحرارة بشكلٍ أساسيٍّ بالسيليزيوس °C أو الكالفن °K)، كما يمكن للحرارة أن تتولّد ضمن المادّة نفسها على حساب أشكال الطاقّة الأخرى (كما في عمليّة تحويل الطاقة الحركية إلى حراريةٍ على سبيل المثال).
يُعتبر الجول (Joule) واحد القياس الدوليّة للحرارة (تختلف عن واحدات درجة الحرارة التي ذكرناها سابقًا) ويكتب "J" اختصارًا، في حين أن واحد الحرارة في النظام المتري هي الكالوري (Calorie) وتُختصر "Cal"، حيث أن 1 كالوري = 4.186 جول.[footnote]،Heat Transfer، من موقع: www.toppr.com، اطّلع عليه بتاريخ 8-11-2019[/footnote]
انتقال الحرارة بالمعنى البسيط
بشكلٍ عام فإن عمليّة انتقال الحرارة تصف تدفّق الطاقة الحرارية بين الجُزيئات المُنفصلة بسبب تفاوت درجات الحرارة فيما بينها. وإن عمليّة الانتقال هذه لا تقتصر فقط على الطاقة، بوصفها طاقةً صرفةً فقط، فقد وجد العلماء أن الانتقال قد يحصل على مستويين آخرين هما الزخم (العمل) والكتلة، بمعنى آخر فإن انتقال الحرارة بين وسطين قد يترافق أيضًا بانتقال كتلة أو زخم أحدهما إلى الآخر.[footnote]،What is Heat Transfer?، من موقع: www.simscale.com، اطّلع عليه بتاريخ 8-11-2019[/footnote]
القانون الثاني في الترموديناميك
ينص القانون الثاني للديناميكيّة الحراريّة على أن الحرارة تنتقل في الحالة السويّة الطبيعية باتجاهٍ واحد، من الأجسام ذات الحرارة الأعلى إلى الأجسام ذات الحرارة الأدنى. ومن أجل عكس هذا القانون لابُد من مؤثّرٍ خارجيٍّ يطبّق عملًا أو جهدًا يفرض انتقال الحرارة من الجسم الأبرد إلى الجسم الأكثر حرارةً. وتُعتبر الثلّاجة مثالًا على هذا الانتقال العكسي المُجبر، حيث تقوم الثلّاجة (بواسطة الطاقة الكهربائية) بامتصاص الحرارة من غرفة التبريد بداخلها (وسط أقل حرارة) وإطلاقها إلى الوسط المحيط (وسط أكثر حرارة).[footnote]،What is Heat Transfer? What is Conduction Heat transfer? What is Convestion Heat Transfer? What is Radiation Heat Transfer?، من موقع: www.brighthubengineering.com، اطّلع عليه بتاريخ 8-11-2019[/footnote]
طرق انتقال الحرارة
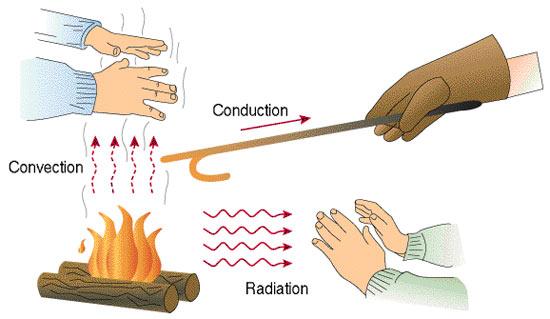
يمكن للحرارة أن تنتقل بثلاث طرقٍ رئيسيةٍ هي التوصيل (conduction) والنقل (convection) والإشعاع (radiation)، يحتاج كلٍ من التوصيل والنقل إلى وجود وسطٍ مادّيٍّ لكي تتمّ عمليّة النقل، على خلاف انتقال الحرارة بالإشعاع والذي لا يحتاج إلى وسطٍ ماديٍّ.
انتقال الحرارة بالتوصيل
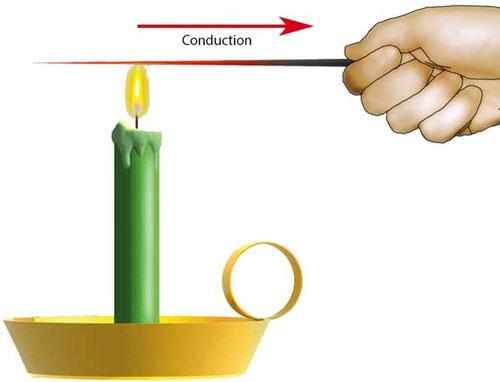
يحدث التوصيل عند تماس جسمين صلبين بدرجات حرارةٍ مختلفةٍ، حيث تنتقل الحرارة من الجسم الأبرد إلى الأدفأ حتى تتساوى درجات الحرارة فيما بينهما. ويمكن تعريف التوصيل بأنّه انتقال الحرارة عبر ارتطام جُزيئات مادّتين مختلفتين حراريًّا. حيث يحدث هذا الاصطدام بين جُزيئات المادة الأولى والثانية في منطقة التماس، فتعطي جُزيئات المادّة الأدفأ، ذات الطاقة الحركية الكبيرة، بعضًا من الطاقة الحركية لجزيئات المادّة الأخرى رافعةً من حرارتها، وهذه الأخيرة تصطدم مع جُزيئات المادّة نفسها ناقلةً الحرارة عبر أجزائها المختلفة.
في الواقع فإن خاصيّة التوصيل تختلف من جسمٍ لآخر، فهناك مواد ذات موصوليّةٍٍ عاليةٍ للحرارة وأخرى ضئيلةٍ. فالأجسام الصلبة مثلًا تتمتّع بناقليةٍ عاليةٍ للحرارة تليها السوائل وأخيرًا الغازات، والتي تُعتبر ذات ناقليّةٍ ضعيفةٍ للحرارة. وهذا في الواقع مرتبطٌ بكثافة جُزيئاتها، فكما نعلم أن جزيئات المادة الصلبة تكون متراصّةً وكثيفةً بخلاف المادّة الغازيّة التي تكون مبعثرةً ومتناثرةً، فيغدو احتمال ارتطام الجزيئات فيها أقل.
من الأمثلة الشائعة لانتقال الحرارة بالتوصيل
هي شعورك بانتقال الحرارة إليك عند لمس الأجسام الدافئ.
انتقال الحرارة بالنقل
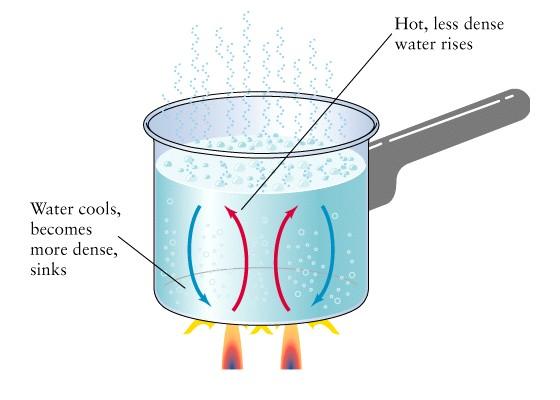
يُعتبر النقل هو النظام السائد في انتقال الحرارة في السوائل والغازات، ويحدث عندما تنتقل الطبقات الأكثر حرارةً في الغازات والسوائل إلى الطبقات الأبرد. وفي الوقت نفسه فإن الطبقات الأبرد تهبط لتأخذ مكان الفراغ التي تركه انتقال الطبقات الساخنة، وهذه الحركة المستمرّة تشكّل نموذجًا ثابتًا من صعود وهبوط الطبقات الدافئة والباردة باستمرار.
ومن أمثلة انتقال الحرارة بالنقل هو تسخين الماء، فعندما تبلغ درجة حرارة الماء 100 درجة مئوية تبدأ الفقاعات الهوائية بالتشكّل أسفل وعاء التسخين، وبإمكانك ملاحظة كيفيّة انتقال هذه الفقاعات إلى الطبقات العليا وهبوط الماء في السطح إلى الطبقات السفلى في الوقت نفسه.
انتقال الحرارة بالإشعاع
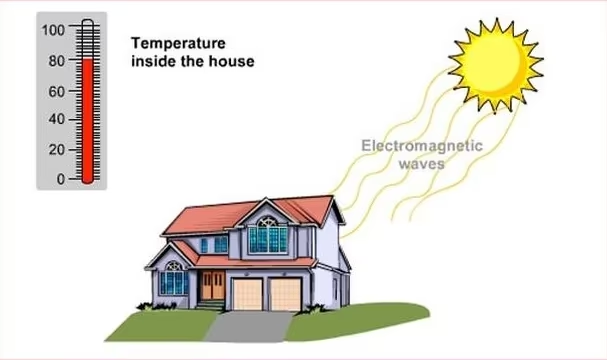
يحتاج كلا التوصيل والنقل إلى وجود وسطٍ ماديٍّ لتنتقل عبره الحرارة بين الأجسام. في حين أن النقل بالإشعاع لا يحتاج إلى وجود وسطٍ ماديٍّ ناقلٍ بين مصدر الحرارة والجسم المُتلقّي لها. فبإمكاننا مثلًا الاحساس بحرارة الشمس على الرغم من أننا بعيدين كل البعد عنها، وذلك لأن الحرارة بإمكانها الانتقال عبر الفراغ الفضائي بواسطة الإشعاع الحراري.
الإشعاع الحراري (يُعرف أيضًا بالأشعة تحت الحمراء) هو في الحقيقة شكلٌ من أشكال الإشعاع الكهرومغناطيسي (أو بمعنى آخر الضوء). والإشعاع بالمعنى العام يصف انتقال الطاقّة على هيئة أمواجٍ كهرومعناطيسيةٍ بسرعة الضوء، وهو لا يحتاج إلى وسطٍ ماديٍّ للانتقال ولا يتطلّب حدوث تبادلًا في كتل المواد.[footnote]،CONDUCTION، من موقع: coolcosmos.ipac.caltech.edu، اطّلع عليه بتاريخ 8-11-2019[/footnote]
الأسئلة الشائعة عن طرق انتقال الحرارة:
هناك ثلاث طرائق لانتقال الحرارة من جسم إلى آخر أو في الجسم نفسه، هي التوصيل conduction والحمل convection والإشعاع radiation.
يوجد ثلاث طرق لانتقال الحرارة عبر الغلاف الجوي: الإشعاع، والتوصيل، والحمل.
تنتقل الطاقة من الشمس إلى الأرض عبر الموجات الكهرومغناطيسية أو الإشعاع. معظم الطاقة التي تمر عبر الغلاف الجوي العلوي وتصل إلى سطح الأرض في شكلين ، الضوء المرئي والأشعة تحت الحمراء.
يسمى انتقال الطاقة الحرارية عن طريق التلامس المباشر، انتقال الحرارة من الجسم الساخن الى الجسم البارد، عن طريق انتشار وتجاذب الجسيمات داخل الجسم، وقد تمر الحرارة من خلال طرق توصيل يتم من خلالها توزيع الحرارة.
1. درجة الحرارة هي كمية يمكن قياسها، بينما الطاقة الحرارية ليست مقدارًا ولا يمكن قياسها.
2. درجات الحرارة تأخذ قيم موجبة وسالبة ويعتمد ذلك على النظام، ولكن الطاقة الحرارية من المستحيل أن تأخذ قيمًا سالبة.
3. وحدة قياس الطاقة الحرارية هي الجول بينما درجة الحرارة يمكن قياسها بالكلفن أو السيلزيوس أو الفهرنهايت.
 LEAP26
LEAP26 ASUS
ASUS RØDE
RØDE REDMAGIC
REDMAGIC TV
TV Partner With Us
Partner With Us