ما هو بيكنج صودا

تم التدقيق بواسطة: فريق أراجيك
بيكنج صودا (Baking Soda) أو صودا الخبز، هو الاسم الشائع لمركب بيكربونات الصوديوم المعروف أيضًا باسم كربونات الصوديوم الحامضية، وصيغته الكيميائية هي (NaHCO3). تعرف بيكربونات الصوديوم أيضًا بأنها ملح الصوديوم لحمض الكربونيك (HCO3)، وتوجد في الطبيعة ويمكن تحضيرها معمليًا، وقد حضَّرها الكيميائي الفرنسي نيكولا لوبلان (Nicolas Leblanc) أول مرة سنة 1791 ميلادية، وبعد حوالي نصف قرن، بدأ إنتاجها صناعيًا حيث أُنشئ أول مصنع لبيكربونات الصوديوم سنة 1846 في الولايات المتحدة.
تركيب بيكنج صودا الكيميائي
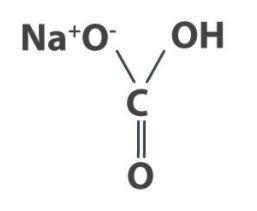
يتكون الجزيء الواحد من بيكنج صودا من أيون صوديوم موجب الشحنة الكهربية، وأيون بيكربونات سالب الشحنة الكهربية كما في الصورة أعلاه، حيث يرتبط أيون الصوديوم الموجب (+Na) عبر رابطة أيونية مع أيون البيكربونات. بالنسبة للروابط الأخرى الموضحة بالصورة، فإنها الروابط داخل البيكربونات ذاتها وهي روابط تساهمية.
الفرق بين الرابطتين الأيونية والتساهمية هو أن الأولى تكون بين الأيونات والثانية بين الذرات، أيضًا تقوم الرابطة الأيونية على مبدأ تخلي إحدى الذرتين عن إلكترون أو أكثر لتصبح أيون موجب (الصوديوم في حالة بيكربونات الصوديوم) في حين تتلقى الأخرى هذا الإلكترون لتصبح أيون سالب (البيكربونات في حالة بيكربونات الصوديوم)، وتنشأ الرابطة عبر الجذب الكهربائي بين الأيونات، في حين تعتمد الرابطة التساهمية على مشاركة الذرات الإلكترونات فيما بينها.
تحضير البيكنج صودا
تتكون بيكربونات الصوديوم عبر التفاعل بين كلوريد الصوديوم (NaCl) والنشادر (NH3) وثاني أكسيد الكربون (CO2) والماء (H2O)، حيث ينتج عن هذا التفاعل مركب كربونات الصوديوم (Na2CO3) الذي يتفاعل بدوره مع الماء وثاني أكسيد الكربون ليكون الناتج النهائي هو بيكربونات الصوديوم أو بيكنج صودا.
NaCl + NH3 + CO2 + H2O → Na2CO3 + NH4Cl
Na2CO3 + CO2 + H2O → 2 NaHCO3
الخواص الكيميائية
يصنف بيكنج صودا كمادة مترددة حيث يسلك سلوك الأحماض والقواعد فيتفاعل مع كليهما، لكن عند ذوبانه في الماء ينتج محلولًا قلويًا ضعيفًا. عند تفاعل بيكربونات الصوديوم مع حمض ينتج ملح الصوديوم للحمض وحمض الكربونيك (H2CO3) الذي يتحلل إلى ماء وثاني أكسيد الكربون. المعادلة التالية تظهر تفاعل بيكربونات الصوديوم مع حمض الهيدروكلوريك (HCl).
NaHCO3 + HCl → NaCl + H2CO3
H2CO3 → H2O + CO2
أما إذا ما تفاعلت مع قلوي فإن الناتج يكون كربونات الصوديوم والماء. توضح المعادلة التالية تفاعل بيكربونات الصوديوم مع هيدروكسيد الصوديوم (NaOH) القلوي:
NaHCO3 + NaOH → Na2CO3 + H2O
تتكسر روابط بيكربونات الصوديوم عند درجة حرارة 50 درجة مئوية، حيث ينتج كربونات الصوديوم والماء وثاني أكسيد الكربون كما في المعادلة التالية:
2NaHCO3 → Na2CO3 + H2O + CO2
الخواص الفيزيائية
يوجد بيكنج صودا في هيئة مسحوق أبيض من البلورات الأحادية، وهو مسحوق عديم الرائحة، يذوب في الماء كما يذوب جزئيًا في بعض المذيبات العضوية كالأسيتون (Acetone) والكحول الميثيلي (Methanol)، في حين لا يذوب في الكحول الإيثيلي (Ethanol). تعتبر بيكربونات الصوديوم قاعدة ضعيفة حيث تصل درجة الأس الهيدروجيني (PH) لها إلى 8.31. تنصهر بيكربونات الصوديوم عند درجة حرارة 50 درجة مئوية، وتبدأ في الغليان عند درجة حرارة 851 درجة مئوية.
الفرق بين بيكنج صودا وبيكنج بودر
إن بيكنج صودا كما سبق وأوضحت، هي بيكربونات الصوديوم القاعدية، أما بيكنج بودر (Baking Powder) فهو ناتج خلط بيكربونات الصوديوم مع حمض جاف عادةً ما يكون حمض الطرطريك (Tartaric). عند استخدام بيكنج صودا يُضاف معها مادة حامضية كالخل أو عصير الليمون، وذلك لمعادلة قاعدية بيكربونات الصوديوم، أما مع البيكنج بودر، فلا نحتاج لإضافة مادة حامضية نظرًا لاحتواء البيكنج بودر ذاته على حمض.
استخدامات وفوائد بيكنج صودا
- طبعًا يستخدم في الخَبز وذلك للمساعدة في تخمر العجين. تتفاعل الصودا مع سائل حمضي يضاف بدوره إلى العجين وينتج عن ذلك فقاعات هواء.
- تنظيف الفواكه والخضروات حيث يزيل نسبة كبيرة من بقايا المبيدات الحشرية الموجودة على الفاكهة، كما يستعمل كمنظف لأوعية الطهي وللملابس والمفروشات وأدوات المنزل والأرضيات، وكذلك كمنظف للحمام.
- إذابة الجليد من الطرقات.
- تستعمل بيكربونات الصوديوم في غسيل الشعر، حيث تتميز بتأثيرها الإيجابي على الشعر كما تساعد على التخلص من القشرة في فروة الرأس.
- يمكن استخدام بيكنج صودا في غسيل الأسنان كبديل عن معجون الأسنان، وقد أظهرت بعض الدراسات أن له تأثير صحي على الأسنان ويمنحها خصائص مضادة للبكتيريا والميكروبات، حيث يزيد الأس الهيدروجيني للعاب، وهو ما يساعد على تثبيط نشاط البكتيريا.
- يمكن استخدامه أيضًا كمزيل للعرق، كما يمكن إضافته إلى صناديق التخزين لمنع تكون رائحة نتيجة إغلاقها لفترة طويلة.
- تخفف بيكربونات الصوديوم الألم الناتج عن لسعات الحشرات.
تأثير بيكربونات الصوديوم على الصحة
ذكرت في الفقرة السابقة أن بيكربونات الصوديوم تستخدم في غسيل الأسنان وعلاج قشرة الشعر، وفيما يلي أضيف إلى ذلك استخدامات وفوائد صحية أخرى لبيكربونات الصوديوم:
- علاج حرقة المعدة: تعمل بيكربونات الصوديوم على معادلة أحماض المعدة حيث تكفي إذابة ما مقداره ملعقة شاي واحدة من بيكربونات الصوديوم في كوب ماء وتناوله، لإيقاف حرقة المعدة، غير أنها قد لا تفلح في بعض الحالات التي لا يكون فيها زيادة أحماض المعدة هو سبب الحرقة، كذلك يجب الحذر عند استخدامها لاحتوائها على نسبة كبيرة من الصوديوم، كما يمكن أن يسبب استخدامها الطويل مشاكل في القلب وفي التمثيل الغذائي.
- تهدئة قُرح الفم: وجد باحثون أن لبيكربونات الصوديوم أثر إيجابي في تهدئة قرح الفم.
- تحسين الأداء الرياضي: أثبتت بعض الأبحاث أن صودا الخبز تسهم في تحسين الأداء الرياضي عبر معادلة حموضة حمض اللاكتيك (Lactic Acid) في الخلايا، والذي تنتجه العضلات في التنفس اللاهوائي ويؤدي تراكمه إلى الاجهاد العضلي.
- تهدئة الحكة وحروق الشمس: يخفف التهيج والألم الناجم عن لسعات الحشرات وحروق الشمس.
- يبطأ تطور أمراض الكِلى المزمنة: أثبتت دراسة أُجريت على 134 شخص بالغ مصاب بمرض الكلى المزمن، أن أولئك الذين يتناولون بيكربونات الصوديوم هم أقل عرضة لتدهور حالتهم بنسبة 36%.
 LEAP26
LEAP26 ASUS
ASUS RØDE
RØDE REDMAGIC
REDMAGIC TV
TV Partner With Us
Partner With Us