ما هو التكافؤ الكيميائي
تم التدقيق بواسطة: فريق أراجيك
أوجد علماء الكيمياء جدولًا يضم كافة العناصر الكيميائية المعروفة مُرتبةً من اليسار إلى اليمين بشكلٍ تصاعديٍّ وفقًا لعددٍ من الاعتبارات منها عدد الإلكترونات الموجودة فيها، لتُساعد في تحديد التكافؤ الكيميائي للعناصر خاصةً تلك الموجودة في المدار الخارجي المحيط بنواة الذرة، والتي تُعتبر أساس التفاعلات الكيميائية بين ذرات العناصر، فما هو التكافؤ الكيميائي وكيف يمكن تحديده بالنسبة للعناصر والمركبات الكيميائية؟
تكافؤ العناصر الكيميائية
يُشير مصطلح التكافؤ الكيميائي للعنصر إلى عدد ذرات الهيدروجين القادرة على الارتباط بذرةٍ واحدةٍ من العنصر أو الحلول محلها، أي بمعنى أدق إن تكافؤ العنصر هو عدد الإلكترونات الموجودة في المدار الخارجي للذرة والتي تحتاجها لإتمام الاتحاد مع ذرات العناصر الأخرى وتُدعى بإلكترونات التكافؤ.
ومع ذلك ليس بالضرورة أن يتساوى تكافؤ الذرة مع عدد إلكترونات التكافؤ في جميع الحالات؛ فمثلًا يمتلك الأكسجين ستة إلكترونات تكافؤ بينما تكافؤه 2.[footnote]، What is Valency?، من موقع: www.freechemistryonline.com، اطّلع عليه بتاريخ 27-10-2019.[/footnote]
مفهوم التكافؤ الكيميائي للعناصر
تمتلك كل ذرةٍ عددًا من الإلكترونات المرتبة في مداراتٍ مختلفةٍ هي K و L و M و N وتدعى الإلكترونات الموجودة في المدار الخارجي بإلكترونات التكافؤ الكيميائي والتي تلعب دورًا هامًّا في أي تفاعلٍ كيميائيٍّ نتيجةً لامتلاكها طاقةً أكبر من الطاقة الموجودة في إلكترونات باقي المدارات.
يحتوي المدار الخارجي في الذرة على 8 إلكترونات كحدٍ أقصى، لكن إن كان ممتلئًا سيؤدي ذلك إلى ضعفٍ في قدرة العنصر على التفاعل حيث تُصبح قدرة الإلكترونات على الاندماج قليلةً للغاية وتكاد تكون معدومةً وهذا ما يُفسر سلوك الغازات الخاملة.
قاعدة الإلكترونات الثمانية
تسعى ذرة العنصر أثناء التفاعل إلى كسب أو التخلي أو مشاركة عددٍ مُحددٍ من الإلكترونات الموجودة في المدار الخارجي حتى تصل إلى ثمانية إلكتروناتٍ فقط؛ فعدد الإلكترونات المكتسبة أو المتشاركة أو المفقودة للوصول إلى ثمانية إلكترونات يُعرف بسعة الذرة الذي يحدد التكافؤ الكيميائي الخاص بها.
مثلًا تحتوي ذرة الهيدروجين في مدارها الخارجي على إلكترونٍ واحدٍ لذلك تحتاج إلى خسارة هذا الإلكترون لتصل إلى الاستقرار ويُصبح عدد الإلكترونات في المدار الخارجي ثمانية وبالتالي يُعتبر التكافؤ الكيميائي للهيدروجين 1، أما المغنيزيوم فيمتلك إلكترونين في مداره الخارجي وعليه أن يفقدهما ليُصبح مُستقرًا ويُحقق قاعدة الثمانية، لذلك يُعتبر تكافؤ المغنيزيوم 2، بينما تمتلك ذرة الفلور 7 إلكترونات في المدار الخارجي ولأنه من الصعب فقدانها كلها تميل الذرة إلى اكتساب إلكترون فيُعتبر تكافؤ الفلور 1 أيضًا.[footnote]، Valency، من موقع: www.toppr.com، اطّلع عليه بتاريخ 27-10-2019.[/footnote]
تحديد التكافؤ الكيميائي من الجدول الدوري
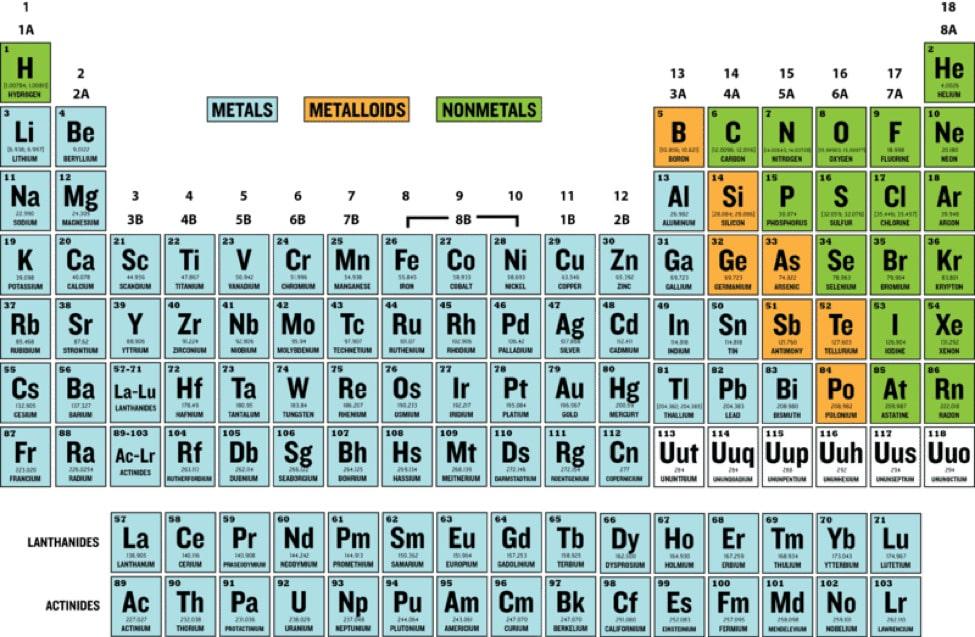
يمكن معرفة عدد إلكترونات تكافؤ العناصر من خلال الجدول الدوري؛ فمثلًا عدد إلكترونات التكافؤ للعناصر الموجودة في العمود 1 مثل الهيدروجين والليثيوم والصوديوم هو إلكترون واحد؛ لذلك تُدعى بالعناصر وحيدة التكافؤ، بينما عدد إلكترونات التكافؤ للعناصر في العمود 2 مثل الكالسيوم والمغنيزيوم والراديوم إلكترونين اثنين وتدعى بالعناصر ثنائية التكافؤ، أما عناصر العمود 7 فهي مُتعددة التكافؤ حيث يبلغ عدد إلكترونات التكافؤ فيها 7، لكن في العمود 18 الذي يضمُّ العناصر الخاملة فإن عدد إلكترونات التكافؤ هو ثمانية وبالتالي يُصبح التكافؤ فيها صفرًا.[footnote]، How can you calculate the valency of each element?، من موقع: www.online-sciences.com، اطّلع عليه بتاريخ 27-10-2019.[/footnote]
تحديد التكافؤ الكيميائي من خلال الصيغ الكيميائية
تعتمد هذه الطريقة على قاعدة الثمانية حيث يمكن تحديد التكافؤ للعديد من العناصر الانتقالية أو الجذور الكيميائية في مركباتٍ محددةٍ من خلال مراقبة طريقة تفاعلها مع عناصر معروفة التكافؤ، عندها تُستخدم طريقة قاعدة الثمانية فالعناصر والجذور الكيميائية تتحد محاولةً الحصول على ثمانية إلكتروناتٍ في مدارها الخارجي حتى تُصبح مستقرةً.
إذا ما أخذنا مركب Nacl، من المعروف أن التكافؤ الكيميائي للصوديوم Na هو 1+ وتكافؤ الكلور Cl هو 1-، فالصوديوم بحاجةٍ للتخلي عن إلكترون والكلور بحاجة لكسب واحدٍ ليستقر المدار الخارجي لديهما، لذلك يُعطي الصوديوم إلكترونًا إلى الكلور وبذلك يتحدد التكافؤ.
عند تطبيق هذه الطريقة على جزيئاتٍ أكثر تعقيدًا لا بد من الأخذ بعين الاعتبار أن العناصر قد تتحد لتُشكّل جذورًا كيميائيةً تفاعليةً لم تتمكن بعد من تحقيق الاستقرار في مدارها الخارجي والحصول على ثماني إلكترونات فيه؛ ومن أمثلة هذه الحالة جذر الكبريتات SO4 وهو جزيءٌ ذو أربع سطوح تتشارك فيه ذرة الكبريت الإلكترونات مع أربع ذرات أكسجين برابطة تُدعى الرابطة التكافؤية.
يتحد مثلًا جذر الكبريت مع الهيدروجين ليتشكل حمض الكبريتيك H2SO4 ويتضمن هذا الجزيء ذرتي هيدروجين تكافؤ كلٍ منها (1+) وبالتالي يكون تكافؤ الجذر (2-).[footnote]، How to Calculate Valency، من موقع: sciencing.com، اطّلع عليه بتاريخ 27-10-2019.[/footnote]
 LEAP26
LEAP26 ASUS
ASUS RØDE
RØDE REDMAGIC
REDMAGIC TV
TV Partner With Us
Partner With Us