العدد الذري
تم التدقيق بواسطة: فريق أراجيك
تاريخ العدد الذري
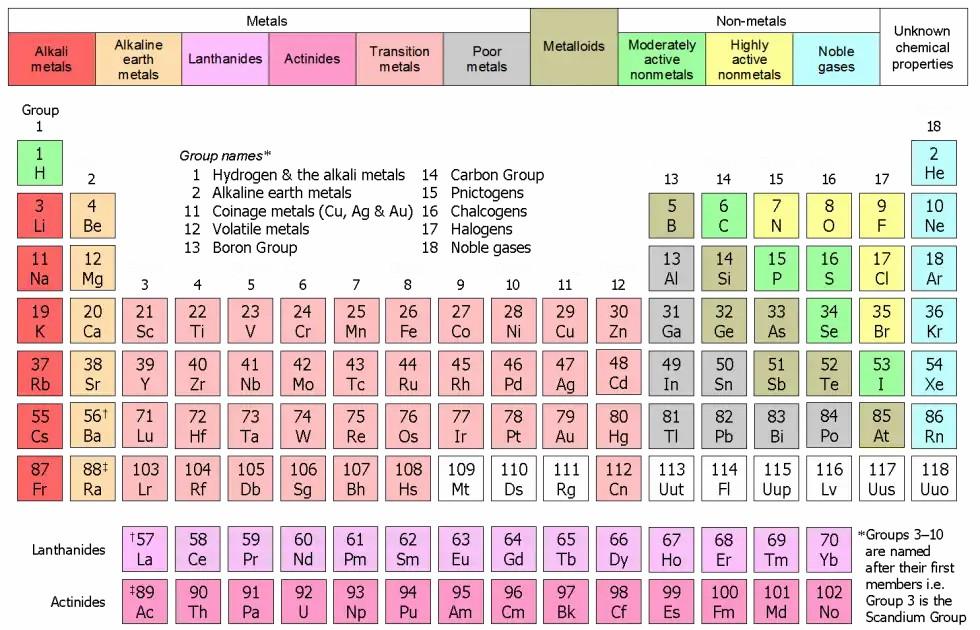
قبل الحديث عن العدد الذري لا بدّ من التعريج قليلًا على الجدول الدوري في الكيمياء، فمعظمنا قد سمع بالجداول الدورية (Periodic Tables) وكيف تم ترتيب العناصر في جدولٍ دوريٍّ بشكلٍ معلوماتيٍّ منظم جدًا. يعود تاريخ الجدول الدوري إلى أواخر العام 1860، بعد اكتشاف ديمتري مندلييف للقانون الدوري Periodic Low، والذي أصبح مباشرةً مفهومًا رئيسيًّا في العلوم الكيميائية، وقد طرأت بعض التعديلات على هذا الجدول، حيث كانت بعض العناصر خارج السياق عند ترتيبها حسب قانون مندلييف.
ولم يستمر الخطأ طويلًا؛ فقد اكتشف فيلهلم رونتجن عام 1895 أشعة X (الأشعة السينية) التي ساعدت العلماء الآخرين على إجراء أبحاثٍ أعمق على اكتشاف مندلييف.
أما مفهوم العدد الذري فقد أُطلق من قبل بحثٍ تاريخيٍّ لهنري غوين والعالم الفيزيائي الإنكليزي جيفريز موسيلي عام 1910، حيث قام الأخير عام 1913 بدراسة الأطوال الموجية بتسليط أشعة X على عددٍ من العناصر الكيميائية، ولاحظ النمط الذي شكلته هذه الأشعة، واكتشف أن الأطوال الموجية لأشعة X المنعكسة تتناقص في نمطٍ منظمٍ قابل للتنبؤ مع زيادة الكتلة الذرية، وافترض موسيلي أن التغير المنتظم في أطوال الموجات من عنصرٍ إلى عنصرٍ يسببه زيادة في الشحنة الموجبة لنواة الذرة تنتقل من عنصرٍ إلى العنصر التالي الأكثر ثقلًا.[footnote]، Atomic Number، من موقع: www.toppr.com، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
أتاح اكتشاف موسيلي إمكانية وضع فهمٍ جديدٍ للقانون الدوري الأول الذي قال فيه مندلييف إن خواص العناصر تختلف بنمطٍ منتظمٍ قابل للتنبؤ به عند ترتيب العناصر حسب كتلتها الذرية، ورغم أنه كان محقًا جوهريًّا، إلّا أن بنية الجدول الدوري على هذا الأساس وقعت بخطأٍ كبيرٍ؛ حيث ظهر أن أزواجًا محددة من العناصر (مثل التيلوريوم والأودين) فقدت مكانها عند ترتيبها حسب كتلها الذرية.
اختفت هذه المشكلة عند استخدام العدد الذري بدلًا من الكتلة الذرية كأساسٍ للجدول الدوري، حيث إن خواص العنصر الكيميائي تعتمد على عدد وترتيب الإلكترونات في ذراتها. بدوره يتم تحديد عدد الإلكترونات في ذرةٍ ما بالشحنة النووية؛ لذا فإنّ عدد البروتونات في النواة (أو الشحنة الحيادية أو العدد الذّرّي) يحدد الخواص الكيميائية للعنصر، وقد شكلت هذه الفرضية أساس العدد الذري، فكل عنصرٍ يملك عددًا فريدًا يشير إلى عدد البروتونات الموجودة في نواة ذرةٍ ما.[footnote]، Atomic Number، من موقع: www.encyclopedia.com، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
معلومات أساسية حول الذرة
- الذرات الحيادية لكل عنصرٍ تحتوي على عددٍ متساوٍ من البروتونات والإلكترونات.
- عدد البروتونات يحدد العددَ الذريَّ لعنصرٍ ما ويستخدم لتمييز العنصر عن الآخر.
- عدد النيوترونات متغيرٌ ما ينتج عنه نظائرٌ؛ وهي أشكالٌ متنوعةٌ من نفس الذرة وتختلف فقط بعدد النيوترونات التي تمتلكها.
- يحدد عدد البروتونات وعدد الإلكترونات معًا العدد الكتلي للعنصر.
- بما أن نظائر العنصر تمتلك عددًا كتليًّا مختلفًا قليلًا، يتم حساب الكتلة الذرية بجمع متوسط الأعداد الكتلية لنظائر هذا العنصر.[footnote]، Atomic Number and Mass Number، من موقع: courses.lumenlearning.com، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
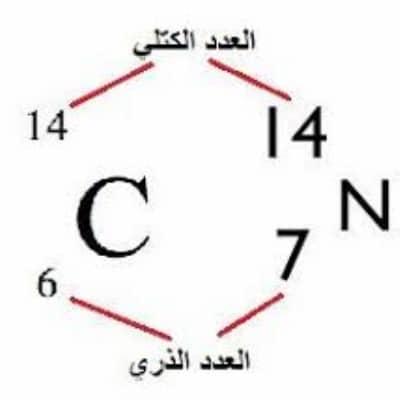
مفهوم العدد الذري
تتكون العناصر الكيميائية من ذراتٍ، كل منها تحمل شحناتٍ إلكترونيةً، وكل ذرةٍ تملك نواةً ثقيلةً نسبيًّا مكونة من بروتونات (ذات شحنةٍ موجبةٍ) ونترونات ( جزئياتٌ حياديةٌ). يوجد في مدار النواة عددٌ من الإلكترونات المشعة الاستثنائية والتي تحمل شحنةً سالبةً متوازنةً مع شحنة البروتونات الموجبة، وتملك الذرات المنتمية إلى ذات العنصر نفس العدد الذري.
يٌعرف العدد الذري بأنه عدد البروتونات في نواة الذرة، وهو مساوٍ لعدد الإلكترونات التي تتحرك حول النواة، وغالبًا ما يُمثل بالرمز Z، وتشكل الذرات التي تتشارك بالعدد الذري ذاته عنصرًا كيميائيًّا.
مثلًا، تحتوي نواة الأكسجين على 8 بروتونات و8 نوترونات، وتبعًا لذلك يكون عدد الأكسجين الذري هو 8؛ حيث إن كل بروتون يحمل شحنةً موجبةً واحدةً، والعدد الذري أيضًا مساوٍ للشحنة الموجبة الكلية لنواة العنصر الذرية.
يمكن قراءة العدد الذري لعنصرٍ مباشرةً من أي جدولٍ دوريٍّ وهو دائمًا العدد الكلي الصغير الموجود مرتبطًا برمز العنصر على الجدول. يكتب الرمز الذري للعنصر في الكيمياء النووية على يسار وأسفل رمز العنصر، ولا يتغير عدد البروتونات لعنصرٍ خاصٍ أبدًا لأنه إن حدث وتغير العدد الذري فإن العنصر بكامله يتغير.[footnote]، Atomic Number، من موقع: www.encyclopedia.com، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
أهمية العدد الذري
- يساعد في تحديد هوية عنصر معين من ذرة.
- يشكل أساس ترتيب العناصر، حيث يتم ترتيب العناصر تصاعديًا حسب الأعداد الذرية لها.
- يساعد في تحديد خواص أي عنصر؛ حيث يحدد الإلكترون التكافؤي سلوك الترابط الكيميائي للعنصر.[footnote]، Atomic Number، من موقع: www.toppr.com، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
البنية الذرية
كما ذكرنا، تتكون الذرات من نوى تحتوي على بروتونات ونيوترونات ومحاطة بالإلكترونات في طبقاتها، ويمكن حساب عدد الجسيمات تحت الذرية في الذرة من العدد الذري للذرة والعدد الكتلي.
ويجب تذكر ما يلي:
- تمتلك كل الذرات المكونة لعنصرٍ معينٍ نفس العدد من البروتونات.
- تمتلك ذرات العناصر المختلفة عددًا مختلفًا من البروتونات.
- تحتوي الذرة على عددٍ متساوٍ من البروتونات والإلكترونات؛ حيث تحمل كل منهما شحنات متساوية ومتعارضة، ما يعني أن الذرات لا تملك شحنةً إلكترونيةً إجمالًا.
مثلًا: العدد الذري للصوديوم هو 11، أي أن كل ذرة صوديوم تملك 11 بروتونًا و11 إلكترونًا؛ أي تملك 11 شحنة موجبة و11 شحنة سالبة.
العدد الكتلي
العدد الكتلي لذرةٍ ما هو العدد الإجمالي من البروتونات والنوترونات، وعادةً تملك ذرات العناصر المختلفة عددًا مختلفًا من العدد الكتلي، لكن قد يكون نفس العدد، وكمثالٍ على ذلك؛ تحمل ذرات الأرغون وذرات الكالسيوم العدد الكتلي نفسه وهو 40.
حساب عدد الجسيمات الذرية
إن رمز الصوديوم هو مربع أصفر اللون ويكتب الرمز Na في المنتصف، أما العدد 23 فيكتب في الزاوية العلوية اليسرى، ورقم 11 في أسفل اليسار، ويمكن أن يُكتب رمز ذرةٍ ما بحيث يظهر عددها الكتلي في الأعلى، وعددها الذري في الأسفل.
لمعرفة أو حساب عدد الجسيمات تحت الذرية في ذرةٍ ما، باستخدام العدد الذري والعدد الكتلي نراعي الآتي:
- عدد البروتونات = العدد الذري.
- عدد الإلكترونات = العدد الذري.
- عدد النيوترونات = العدد الكتلي - العدد الذري.[footnote]، Atomic structure، من موقع: www.bbc.co.uk، اطّلع عليه بتاريخ 7-10-2019.[/footnote]
 LEAP26
LEAP26 ASUS
ASUS RØDE
RØDE REDMAGIC
REDMAGIC TV
TV Partner With Us
Partner With Us